Сокращения: EASL — Европейская ассоциация по изучению печени; EMA — Европейское агентство по лекарственным средствам; FDA — Управление по контролю за качеством пищевых продуктов и лекарственных средств США; HBcAg — сердцевинный антиген вируса гепатита B; HBsAg — поверхностный антиген вируса гепатита B; ВГВ — вирус гепатита B; ВГС — вирус гепатита C; АлАТ — аланинаминотрансфераза; IFN — интерферон; НА — нуклеоз(т)идные аналоги; пгРНК — прегеномная РНК; ПППД — противовирусные препараты прямого действия; ПЦР — полимеразная цепная реакция.
Европейская ассоциация по изучению печени (EASL) опубликовала рекомендации по лечению гепатитов C и B [1, 2]. Безинтерфероновая терапия противовирусными препаратами прямого действия (ПППД) сегодня служит стандартом лечения гепатита C на всех стадиях болезни, однако связана с риском реактивации вируса гепатита В (ВГВ) как у HBsAg-позитивных, так и у HBsAg-негативных пациентов со скрытым гепатитом B [3]. Реактивация ВГВ у пациентов с гепатитом C, получающих лечение ПППД, биологически возможна, поскольку ПППД прекращают репродукцию вируса гепатита С (ВГС), удаляя его из гепатоцитов в течение нескольких недель, если не дней, в зависимости от эффективности неспецифического противовирусного иммунного ответа. В связи с этим любое прямое вмешательство ВГС в репродукцию ВГВ внезапно блокируется, вызывая потенциальное нарушение равновесия при наличии внутрипеченочного репродуктивного пространства для последнего. Более того, гепатоцеллюлярная регенерация вследствие элиминации ВГС может еще больше расширить количество клеток, доступных для инфицирования ВГВ. Этот эффект был менее выражен при терапии на основе интерферона (IFN) за счет свойственной IFN активности против ВГВ [4]; отсутствие действия ПППД, направленных против ВГС, на ВГВ означает, что этот вопрос сегодня вызывает беспокойство и ведет к соответствующим предупреждениям от Управления по контролю за качеством пищевых продуктов и лекарственных средств США (FDA) и Европейского агентства по лекарственным средствам (EMA).
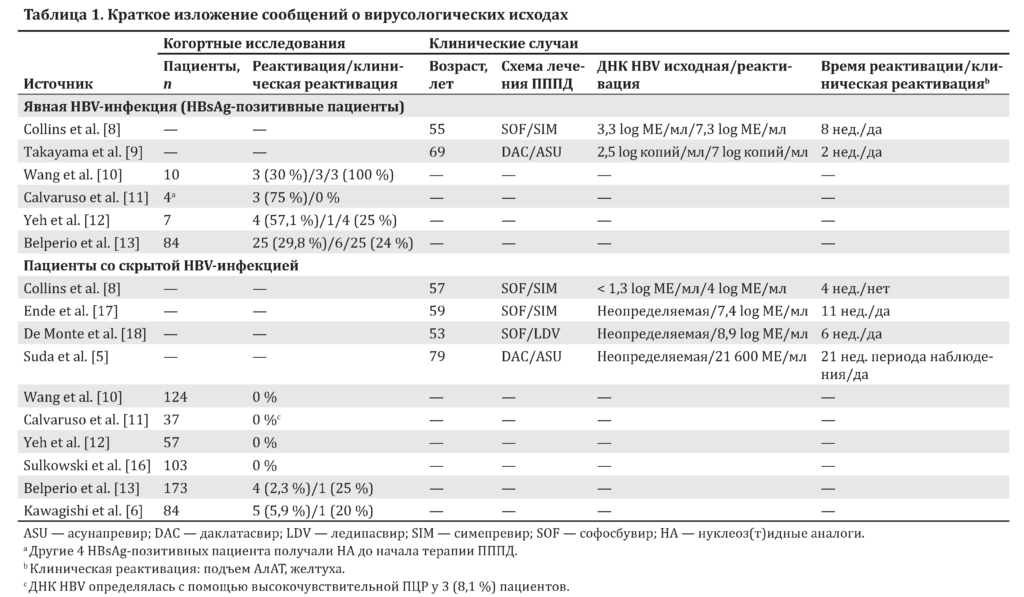
Suda et al. [5] и Kawagishi et al. [6] сообщают о новых случаях реактивации ВГВ у пациентов с гепатитом C, получающих лечение ПППД. Чтобы прояснить риск реактивации и оценить наилучший подход к лечению таких пациентов, необходимо разделение между двумя различными группами пациентов с гепатитом C: теми, у кого гепатит B очевиден (HBsAg-позитивные), и теми, у кого инфекция ВГВ скрыта (по большей части позитивность по антителам к HBcAg в отсутствие HBsAg).
Явная ВГВ-инфекция (HBsAg-позитивные пациенты)
В целом распространенность смешанной инфекции, вызванной ВГВ и ВГС, колеблется от 2 до 10 % у пациентов, позитивных на антитела к ВГС [7]. На заре безинтерфероновой эры некоторые группы ученых сообщали о реактивации ВГВ у лиц со смешанной инфекцией, получающих ПППД [8–11]. Collins et al. [8] описали пациента со смешанной инфекцией, у которого после 8 нед. применения софосбувира и симепревира имел место подъем активности аланинаминотрансферазы (АлАТ) до 1495 МЕ/л и появилась желтуха (общий билирубин 12,2 мг/дл). Takayama et al. описывали реактивацию ВГВ на 15-е сутки применения даклатасвира и асунапревира с подъемом активности АлАТ до 237 МЕ/мл и повышением уровня ДНК ВГВ с 2,5 до 7 log копий/мл [9]. В обоих случаях терапия нуклеоз(т)идными аналогами (НА) купировала обострение гепатита B. После этих случаев FDA и EMA выпустили предупреждения о риске реактивации у пациентов, получающих ПППД по поводу гепатита C (сообщение FDA по безопасности препаратов «Реактивация ВГВ у некоторых пациентов, получающих ПППД для лечения гепатита C» от 4 октября 2016 г. и информационное письмо EMA 263596/2016 от 5 апреля 2016 г.).
После сообщений о первом случае 4 обсервационных исследования проанализировали распространенность явной ВГВ-инфекции у пациентов с гепатитом C, которых планировали лечить ПППД, и оценили частоту реактивации ВГВ. Wang et al. сообщили о распространенности 3,1 % у пациентов, позитивных на HbsAg, из группы 327 пациентов, получающих ПППД для приема внутрь для лечения гепатита C. 3 (30 %) из 10 пациентов, позитивных на HBsAg, имели гепатит: один — без желтухи, другой — с желтухой и третий — с печеночной недостаточностью; и все эти случаи были связаны с реактивацией ВГВ [10]. Второе исследование [11] сообщило о 8 (7,7 %) случаях у пациентов, позитивных на HBsAg из группы 104 пациента с гепатитом C и циррозом, получавших лечение ПППД. 4 пациента получали НА и оставались негативными на ДНК ВГВ во время и после терапии гепатита C. 3 (75 %) из 4 неактивных носителей, оставленных без лечения по поводу гепатита B на момент начала терапии ПППД, стали позитивными на ДНК ВГВ в течение первых 4 нед. терапии гепатита C, и уровень ДНК ВГВ у них вырос на 2–3 log без биохимических признаков обострения. Немедленно была начата терапия НА и достигнуто подавление ДНК ВГВ.
Третье исследование за авторством Yeh et al. [12] проанализировало 64 пациентов с хроническим гепатитом C с ВГВ-инфекцией в настоящем (7 пациентов) и прошлом (57 пациентов). Из 7 пациентов с текущей ВГВ-инфекцией вирусологическая реактивация ВГВ была обнаружена у 4 (57,1 %); 1 пациент имел клиническую реактивацию ВГВ, которая прошла после назначения энтекавира. В самом последнем исследовании, проведенном Belperio et al. [13], были ретроспективно оценены 62 290 больных гепатитом С после завершения терапии ПППД. Из 377 (0,6 %) пациентов, которые были HBsAg-позитивными до начала терапии ПППД, 96 (25,5 %) получали лечение от гепатита B на момент начала терапии ПППД.
Во время лечения ПППД тестирование на ДНК ВГВ было проведено у 22,3 % (84 из 377) пациентов, позитивных на HBsAg, и у 30 (35,7 %) из них ДНК ВГВ определялась.
Всего у 25 (29,8 %) пациентов имело место повышение уровня ДНК ВГВ, у 8 пациентов была реактивация ВГВ, определяемая как повышение уровня ДНК ВГВ > 1000 МЕ/мл от исходного, 6 из них также имели высокую активность аминотрансфераз. На эту тему также опубликован метаанализ [14]. Авторы сравнили пациентов с гепатитом C и явной ВГВ-инфекцией, получавших IFN vs ПППД, и сделали вывод, что объединенная частота реактивации ВГВ была одинаковой у пациентов, получавших терапию на основе IFN и ПППД (14,5 vs 12,2 %), но у пациентов, получавших ПППД, она возникала значительно раньше (во время лечения), чем у пациентов, получавших терапию на основе IFN (в конце лечения и во время периода наблюдения).
Исходя из этих данных, EASL рекомендует рассматривать пациентов, позитивных на HBsAg, получающих терапию ПППД, как кандидатов на одновременную профилактику с помощью НА и требующих тщательного наблюдения (степень рекомендации 2). Однако следует заметить, что большинство пациентов с ВГС/ВГВ-коинфекцией и выраженным поражением печени получают эффективную терапию НА, что устраняет риск реактивации.
Пациенты со скрытой ВГВ-инфекцией (по большей части позитивные на антитела к HBcAg в отсутствие HBsAg)
Оценки риска реактивации ВГВ у пациентов с гепатитом C и предшествовавшим контактом с ВГВ более противоречивы, а рекомендации менее строги. Возможности, предлагаемые ПППД в лечении пациентов с тяжелым поражением печени, имеющих высокую вероятность носительства скрытой ВГВ-инфекции, делают вопрос еще более релевантным. Действительно, доля пациентов с хроническим гепатитом C и серологическими свидетельствами предшествующего контакта с ВГВ, определяемыми наличием антител к HBcAg в отсутствие HBsAg, колеблется от 30 до 60 % [7, 15].
Данные первых 3 когортных исследований, проведенных с учетом этих обстоятельств, могут быть суммированы следующим образом: эпизодов вирусологической реактивации ВГВ во время терапии ПППД не было у 124, 37 и 57 пациентов с инфекцией ВГВ в прошлом, наблюдавшихся Wang et al., Calvaruso et al. и Yeh et al. соответственно. Дальнейший анализ с использованием высокочувствительной ПЦР показал определяемый уровень ДНК ВГВ у 8 % пациентов итальянской когорты [11]. Кроме того, анализ образцов сыворотки 103 пациентов, ранее инфицированных ВГВ и пролеченных в клиническом исследовании ледипасвира-софосбувира в Тайване и Корее, не обнаружил ни одного случая реактивации ВГВ [16]. Согласно этим результатам, мы можем сделать вывод, что реактивация ВГВ не представляет проблему у пациентов без активного гепатита B.
Однако 2 наблюдения в Японии (1 клинический случай и 1 когортное исследование) содержат новейшие сообщения о реактивации ВГВ у пациентов, излеченных от гепатита B [8, 17, 18].
Suda et al. [5] сообщают о случае у 79-летней женщины, инфицированной ВГС генотипа 1b, у которой случилась реактивация ВГВ через 21 нед. после эрадикации ВГС с помощью ПППД. Исходная оценка показала, что пациентка была HBsAg-негативна, имела антитела к HBsAg и HBcAg и неопределяемый уровень ДНК ВГВ. В отличие от прежде опубликованных сообщений, показавших, что репродукция ВГВ происходит в первые недели терапии ПППД, в данном случае наблюдалась поздняя реактивация ВГВ. Авторы измерили количество прегеномной РНК (пгРНК), транскрибируемой с генома ВГВ в образцах печени, полученных до начала терапии ПППД. Они выявили пгРНК ВГВ как до, так и после лечения даклатасвиром/асунапревиром, что подтверждает диагноз реактивации.
Kawagishi et al. [6] проанализировали данные 84 пациентов, которые были излечены от гепатита B (HBsAg- и ДНК ВГВ-негативные и позитивные на антитела к HBcAg и HBsAg), и выявили 5 (5,9 %) случаев с определяемой ДНК ВГВ во время лечения, но только 1 случай с повышением активности аминотрансфераз.
Несмотря на то что гепатит, вызванный реактивацией ВГВ, не наблюдался, 2 пациента с повторным появлением ВГВ и эрадикацией ВГС имели виремию ВГВ на 8-й и 12-й неделях после завершения терапии соответственно, что позволяет предположить персистенцию репродукции ВГВ после элиминации ВГС. В этом исследовании пациенты были старше 65 лет и не имели факторов иммунной недостаточности. Ретроспективное исследование, проведенное Belperio et al. [13], показало частоту определяемости ДНК ВГВ 2,3 % (4 из 173 пациентов) у пациентов, позитивных только на антитела к HBcAg на фоне терапии ПППД.
Клинически реактивация ВГВ часто протекает легко. Между тем в 2015 г. у 59-летней женщины с хроническим гепатитом C генотипа 1b и изолированной позитивностью на антитела к HBcAg, начавшей лечение симепревиром, софосбувиром и рибавирином, развилась фульминантная форма реактивации ВГВ , приведшая к трансплантации печени на 11-й неделе запланированного 12-недельного курса [17]. В силу ранее обсуждавшихся данных пациентам, позитивным на антитела к HBsAg и HBcAg, показан мониторинг активности сывороточных аминотрансфераз.
В заключение отметим, что реактивация ВГВ — частое явление у пациентов со смешанной инфекцией, вызванной ВГВ и ВГС, но она может возникать и у пациентов, излечившихся от гепатита B (табл. 1). Таким образом, пациентов важно проверять на HBsAg, антитела к HBcAg и HBsAg, чтобы назначить терапию НА, если определяется HBsAg или если ДНК ВГВ определяется у пациентов со скрытым гепатитом B. Низкий риск реактивации у пациентов, ранее контактировавших с ВГВ, позволяет ограничиться отслеживанием активности сывороточных аминотрансфераз и оценкой уровня ДНК ВГВ в случае повышения активности печеночных ферментов.
Реактивация ВГВ часто происходит во время терапии гепатита C ПППД, однако описаны и случаи поздней реактивации (после окончания терапии), что означает, что нужно продолжать наблюдение пациентов после элиминации ВГС. Схемы ПППД и генотип ВГС, по-видимому, не влияют на риск реактивации. В литературе не описаны случаи реактивации ВГВ у пациентов с недостаточностью иммунитета, и роль количественного уровня HBsAg у HBsAg-позитивных пациентов остается неясной.
Целесообразны дальнейшие исследования, направленные на выявление надежных прогностических факторов реактивации ВГВ.
Конфликты интересов
VC — гранты на поездки; выступления и участие в консультативных комиссиях для компаний AbbVie, BMS, Gilead Sciences и Intercept; грант и поддержка исследований от MSD.
AC — исследовательские гранты, гонорары за чтение лекций, участие в консультативных комиссиях, научные консультации для компаний Abbvie, Gilead Sciences, BMS, MSD, Intercept.
Дополнительные материалы
Дополнительные материалы к статье представлены в англоязычном приложении на сайте https://dx.doi.org/10.1016/j.jhep.2017.08.017.
Литература
- European Association for the Study of the Liver. EASL recommendations on treatment of hepatitis C 2016. J Hepatol 2017;66:153–194.
- European Association for the Study of the Liver. EASL 2017 Clinical Practice Guidelines on the management of hepatitis B virus infection. J Hepatol 2017;67:370–398.
- Raimondo G, Allain JP, Brunetto MR, et al. Statements from the Taormina expert meeting on occult hepatitis B virus infection. J Hepatol 2008;49:652–657.
- Villa E, Grottola A, Trande P, et al. Reactivation of hepatitis B virus infection induced by interferon (IFN) in HBsAg-positive, anti-HCV-positive patients. Lancet 1993;341:1413.
- Suda T, Shimakami T, Shirasaki T, et al. Reactivation of hepatitis B virus from an isolated Anti-HBc positive patient after eradication of hepatitis C virus with direct-acting antiviral agents. J Hepatol 2017;67:1108–1111.
- Kawagishi N, Suda G, Onozawa M, et al. Hepatitis B virus reactivation during hepatitis C direct-acting antiviral therapy in patients with previous HBV infection. J Hepatol 2017;67:1106–1108.
- Bini EJ, Perumalswami PV. Hepatitis B virus infection among American patients with chronic hepatitis C virus infection: prevalence, racial/ethnic differences, and viral inter-actions. Hepatology 2010;51:759–766.
- Collins JM, Raphael KL, Terry C, et al. Hepatitis B virus reactivation during successful treatment of hepatitis C virus with sofosbuvir and simeprevir. Clin Infect Dis 2015;61:1304–1306.
- Takayama H, Sato T, Ikeda F, Fujiki S. Reactivation of hepatitis B virus during interferon-free therapy with daclatasvir and asunaprevir in patient with HBV/HCV co-infection. Hepatol Res 2015.
- Wang C, Ji D, Chen J, Shao Q, et al. Hepatitis due to reactivation of hepatitis B virus in endemic areas among patients with hepatitis C treated with direct-acting antiviral agents. Clin Gastroenterol Hepatol 2017;15:132–136.
- Calvaruso V, Ferraro D, Licata A, et al. HBV reactivation in patients with HCV/HBV cirrhosis on treatment with direct acting antivirals. J Viral Hepat 2017.
- Yeh ML, Huang CF, Hsieh MH, et al. Reactivation of hepatitis B in patients of chronic hepatitis C with hepatitis B virus infection treated with direct acting antivirals. J Gastroenterol Hepatol 2017.
- Belperio PS, Shahoumian TA, Mole LA, Backus LI. Evaluation of hepatitis B reactivation among 62,920 veterans treated with oral hepatitis C antivirals. Hepatology 2017;66:27–36.
- Chen G, Wang C, Chen J, Ji D, Wang Y, Wu V, et al. Hepatitis B reactivation in hepatitis B and C coinfected patients treated with antiviral agents: a systematic review and meta-analysis. Hepatology 2017;66:13–26.
- Tyson GL, Kramer JR, Duan Z, Davila JA, Richardson PA, El-Serag HB. Prevalence and predictors of hepatitis B virus coinfection in a United States cohort of hepatitis C virus-infected patients. Hepatology 2013;58:538–545.
- Sulkowski MS, Chuang W-L, Kao J-H, Yang JC, Gao B, Brainard DM, et al. No evidence of reactivation of hepatitis B virus among patients treated with ledipasvir-sofosbuvir for hepatitis C virus infection. Clin Infect Dis 2016;63:1202–1204.
- Ende AR, Kim NH, Yeh MM, et al. Fulminant hepatitis B reactivation leading to liver transplantation in a patient with chronic hepatitis C treated with simeprevir and sofosbuvir: a case report. J Med Case Rep 2015;9:164.
- De Monte A, Courjonb J, Anty R, et al. Direct-acting antiviral treatment in adults infected with hepatitis C virus: Reactivation of hepatitis B virus coinfection as a further challenge. J Clin Virol 2016;78:27–30.
Похожие статьи:
- После излечения гепатита С печень не восстанавливается
Сегодня пациенты с гепатитом С могут полностью излечиться. Цель лечения – отсутствие РНК вируса в…
- Как предотвратить рецидив гепатита Б после Тенофовира
Ученые обнаружили важный предиктор рецидива гепатита В у пациентов, прекративших курс лечения тенофовиром. В исследовании…
- ПППД вылечивают не всех афроамериканцев от гепатита С
Вероятность достижения устойчивого вирусологического ответа среди афроамериканских пациентов была значительно ниже по сравнению с белыми…
Имеются противопоказания! Необходима консультация специалиста