Введение
Применение противовирусных препаратов прямого действия (ПППД) произвело революцию в лечении пациентов с хроническим вирусным гепатитом C (ВГС). Показатели эффективности лечения в сочетании с высоким комфортом и низким уровнем побочных эффектов способствуют высокому распространению безинтерфероновых схем в Европе. Данные преимущества особо подчеркиваются с учетом того, что не было ни одного из положительных аспектов в эпоху интерферона. Несмотря на высокую эффективность безинтерфероновых схем лечения, в литературе описаны случаи рецидива гепатоцеллюлярной карциномы (ГЦК) и случаи диагностики de novo после успешного лечения ВГС с использованием ПППД. Данное наблюдение вызывает сомнения относительно того, могут ли эти препараты каким-либо образом влиять на появление гепатокарциномы.
В данной статье мы описываем два случая пациентов, проходивших лечение ПППД, у которых развилась гепатоцеллюлярная карцинома.
Клинические случаи
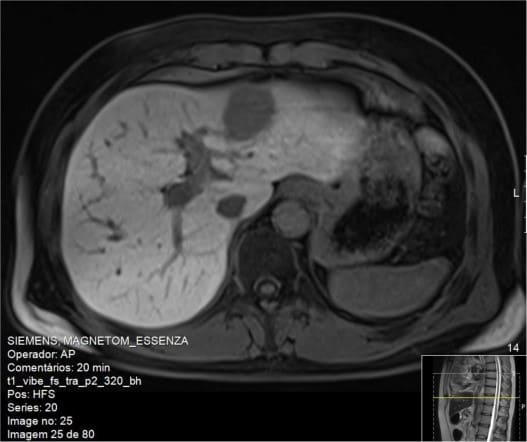
Пациентом 1 был 52-летний мужчина с умеренным потреблением алкоголя в анамнезе, ранее употреблявший наркотические средства внутривенным путем, имеющий факторы риска болезней системы кровообращения (сахарный диабет 2 типа, артериальная гипертензия и дислипидемия) и хроническим ВГС (генотип 3а), диагностированным в 1997 году. Осложнениями ВГС являлись вторичный гемохроматоз и пролиферативный мембранозный гломерулонефрит. Эластография печени показала значения, соответствующие степени фиброза печени F4 по шкале METAVIR. В 2011 году он завершил 24-недельную терапию пегилированным интерфероном и рибавирином и продемонстрировал быстрый вирусологический ответ. Тем не менее, во время последующего наблюдения биохимические данные говорили о процессах цитолиза. Приблизительно через три месяца после окончания терапии подтвердилась её неэффективность. В период с апреля по октябрь 2015 года данный пациент прошел 24 недельный курс лечения ледиспавиром, софосбувиром и рибавирином, достигнув устойчивого вирусологического ответа. Спустя 24 недели после окончания терапии ВГС не определялся, но при прохождении планового УЗИ брюшной полости было выявлено гетерогенное узловое образование в левой доле 43 на 32 мм. Это образование отсутствовало на УЗИ выполненном до начала лечения. Дополнительная магнитно-резонансная томография позволила предположить аденому печени (рис. 1), но биопсия печени показала наличие гепатоцеллюлярной карциномы. В то время уровень альфа-фетопротеина в сыворотке крови составлял 204,20 МЕ / мл. Пациент был подвергнут 2/3 бисегментэктомии. Гистологическое исследование выявило наличие хорошо дифференцированной гепатоцеллюлярной карциномы с признаками лимфатососудистой инвазии на расстоянии 3 мм от операционного края (pT2NxR0).
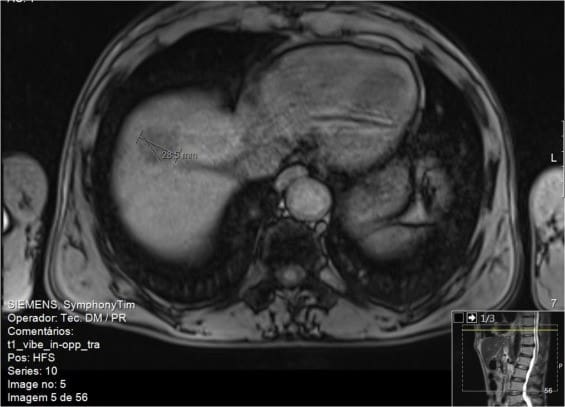
Пациент 2. Мужчина, 58 лет, с активным злоупотреблением алкоголем, курением (более 44 лет), бывший инъекционный наркоман (употреблял кокаин и героин внутривенно, в возрасте с 14 до 40 лет). ВГС (генотип 1а) был диагностирован в 2013 году. Осложнения представляли собой позднюю кожную порфирию и вторичный гемохроматоз при флеботомиях. Эластография печени показала значения фиброза печени F4 по шкале METAVIR. В 2014 году на УЗИ брюшной полости было обнаружено новообразование, которое по подозрениям представляло собой гемангиому правой доли печени. При проведении МРТ было установлено, что данное образование является лишь областью перфузионного изменения сегментов VII / VIII. В 2015 году пациент завершил 24 недельный курс лечения ледиспавиром и софосбувиром. На 24 неделе был достигнут устойчивый вирусологический ответ и исчезновением кожной порфирии. Спустя 13 месяцев после окончания лечения на магнитно-резонансной томографии был обнаружен узелок размером 29 мм в сегментах VII/VIII с подозрением на гепатоцеллюлярную карциному (рис. 2). Гистологическое исследование показало хорошо дифференцированную гепатоцеллюлярную карциному с обширными областями некроза, и признаками, указывающими на внутриопухолевую лимфо-сосудистую инвазию с отсутствием признаков сегментарной лимфо-сосудистой инвазии; минимальный хирургический запас составлял 5 мм (pT2NxR0).
Обсуждение
Очевидно, что при сравнении с предыдущими схемами лечения, основанными на пегилированном ИФН и рибавирине, лекарственные средства, используемые в настоящее время для лечения ВГС, имеют показатели достижения устойчивого вирусологического ответа более 95%. К моменту достижения УВО во многих случаях наблюдается значительное снижение фиброза печени, а также увеличение общей выживаемости (в основном связанные с предотвращением декомпенсации заболеваний печени, снижением необходимости трансплантации и риска возникновения или рецидива ГЦК). Что касается ГЦК, эта связь логично прослеживается, учитывая, что цирроз печени является основным фактором риска развития ГЦК, а в свою очередь хронический гепатит С является одной из наиболее частых этиологических причин развития цирроза, с риском развития ГЦК у на фоне гепатита С, который оценивается приблизительно на уровне 8%. Принимая во внимание вышеизложенное, можно ожидать, что ПППД позволит снизить частоту возникновения и рецидивов ГЦК. Тем не менее, после описания случаев рецидива ГЦК у пациентов, получавших эти препараты, мнения многих врачей разошлись, что вызвало споры и даже предположение, о том, что ПППД может способствовать развитию этой неоплазии.
Данный вывод можно объяснить несколькими аспектами. С одной стороны, известно, что даже после достижения УВО риск ГЦК, хотя и существенно снижается, но сохраняется у пациентов с циррозом печени, как в случаях, описанных здесь. С другой стороны, ПППД позволяет проводить лечение пациентов на более поздних и запущенных стадиях вирусного гепатита С, которые в сочетании с многочисленными осложнениями и метаболическими нарушениями, сами по себе имеют более высокий риск развития ГЦК. В патофизиологическом отношении было высказано предположение, что ПППД может привести к дерегуляции иммунного ответа, связанного с высокой скоростью снижения вирусной нагрузки ВГС. Благодаря различным механизмам, включая отсутствие активации эндогенного интерферона и резкое сокращение Т-киллеров, ПППД, возможно, способствуют более интенсивному прогрессированию ГЦК на фоне сформировавшихся патологий.
Также было высказано предположение, что некоторые биомаркеры могут быть важными факторами прогноза риска ГЦК после лечения ВГС. Например, в одном из исследований было показано, что фактор роста эндотелия сосудов значительно увеличился во время и после лечения ПППД, хотя другие исследования указывают на то, что такое увеличение может играть роль маркера среди пациентов и с другими вариантами предрасположенности к ГЦК. Несмотря на то, что на сегодняшний день опубликовано несколько исследований, в которых предпринята попытка оценить наличие более высокого риска возникновения и/или рецидива ГЦК после применения ПППД по сравнению с ИФН, пока нет достаточных данных, подтверждающих разницу между этими двумя группами пациентов.
В данной статье мы описали два клинических случая пациентов с ВГС и признаками цирроза печени, у которых был диагностирован ГЦК вскоре после лечения ПППД, хотя вполне возможно, что у обоих пациентов уже присутствовали небольшие новообразования, но малый размер не позволил обнаружить их ранее.
Заключение
В отсутствие данных, подтверждающих прямую связь между использованием ПППД и развитием ГЦК, существует явное преимущество для всех пациентов с ВГС. Тем не менее, постоянное выявление новых случаев, таких как были представлены здесь, подчеркивает необходимость дальнейших исследований, в том числе многоцентровых и проспективных. В частности, в краткосрочной перспективе может быть проведена оценка потенциальных биологических маркеров, которые вместе с клиническими данными помогут выявить пациентов с повышенным риском развития ГЦК после лечения ПППД.
Источник:
Hepatocellular carcinoma after direct-acting antiviral therapy for chronic HCV infection: Is it a real risk?
IDCases
Volume 14, 2018 , e00450
https://doi.org/10.1016/j.idcr.2018.e00450
Коллектив авторов:
Cátia Dias, Filipa Duarte-Ribeiro
Department of Internal Medicine, Centro Hospitalar de Vila Nova de Gaia / Espinho, Portugal
Остались вопросы? Получите ответ на форуме
Имеются противопоказания! Необходима консультация специалиста.