Введение
Вирусный гепатит С (ВГС) является одной из основных причин широкой группы метаболических нарушений и хронических заболеваний печени во всем мире. Воспаление, вирусной этиологии зачастую приводит к развитию фиброза печени, циррозу и грозным отдаленным осложнениям, таким как гепатоцеллюлярная карцинома. Во многом, своевременное лечение имеет важное значение, поскольку купирование воспалительного и регресс фибротических процессов существенно снижает смертность связанную с данной инфекцией.
В течение многих лет терапия ВГС состояла из различных комбинаций на основе пегилированного интерферона и рибавирина с длительностью от 24 до 48 недель. При таком подходе пациенты с 1 генотипом достигали устойчивого вирусологического ответа (УВО) только 50% клинических случаев. Несмотря на различные попытки поиска варианта фармакологического усиления, например использование ингибиторов протеаз бустированных ритонавиромом в комбинации с пегилированным интерфероном, все варианты сопровождалось многочисленными побочными эффектами, такими как:
- анемия
- лейкопения
- тромбоцитопения
- гриппоподобные симптомы
- изменениями уровня глюкозы в крови, функций щитовидной железы
- тревожностью, расстройствами эмоциональной сферы и различными аутоиммунными нарушениями.

Для преодоления множества препятствий были разработаны таргетированные препараты нового поколения, известные как ПППД или противовирусные препараты прямого действия. Их широкое распространение и возможность использование без интерферона существенно улучшало эффективность и безопасность лечения, уменьшая побочные эффекты, что особенно важно для пациентов с цирротическими изменениями и множеством сопутствующих заболеваний, как наиболее восприимчивым и чувствительным группам. В клинической практике Бразилии наиболее часто используемыми ПППД являются софосбувир (нуклеотидный аналог ингибитора РНК-полимеразы), даклатасвир (ингибитор NS5A) и симепревир (ингибитор протеазы NS3-4A).
На данный момент уже накоплены различные сообщения о побочных эффектах данных препаратов — большая часть из них, переносятся удовлетворительно и не требуют прекращения лечения или коррекции в условиях стационара. Однако, некоторая часть из них, невзирая на статистически достоверную редкость, могут быть серьезными и иметь значительные отдаленные последствия. В данной статье мы сообщаем о случае возникновения ладонно-подошвенного синдрома (эритродизестезия) вызванного лечением ВГС с использованием ПППД.
Клинический случай
49-летний мужчина с циррозом печени смешанной этиологии, на фоне 1 генотипа ВГС и злоупотребления алкоголем был направлен для проведения лечения в нашу клинику. Данный пациент ранее не проходил лечение ВГС, на момент поступления имел ряд сопутствующих заболеваний: артериальную гипертензию, сахарный диабет, тревожное расстройство и злоупотреблял табакокурением. Согласно объективным данным истории болезни как до лечения так и ранее у него не наблюдалось желудочно-кишечного кровотечения, асцита и печеночной энцефалопатии.
Не смотря на высокое значение жесткости печени по данным Fibroscan® (47,2 кПа, F4) функции были компенсированы (Child-Pugh A, MELD 6), при этом проведенное УЗИ и эндоскопия выявили портальную гипертензию с варикозным расширением вен пищевода. Значения базовых лабораторных исследований были следующими: гемоглобин: 15 мг/дл, лейкоциты: 8,710/мм3 , количество тромбоцитов: 193, общий билирубин: 0,99 мг/дл [контрольное значение (RV)<1,2], мочевина: 41 мг/дл (RV <43), креатинин: 0,9 мг/дл (RV<1,2), аланинаминотрансфераза: 82 МЕ/л (RV<50), аспартатаминотрансфераза: 48 МЕ/л (RV<50), щелочная фосфатаза: 117 МЕ / л (RV <120), гамма-глутамилтрансфераза: 300 МЕ/л (RV<38), альбумин: 4,0 г/дл (RV 3,5-5,2), INR: 0,9 (RV <1,25). Вирусная нагрузка ВГС составила 6,91 log. Качественное определение сывороточного криоглобулина было положительным без каких-либо клинических проявлений.
Данному пациенту была назначена схема лечения с использованием софосбувира (400 мг), симепревира (150 мг) и рибавирина (1000 мг) длительностью двенадцать недель. На шестой неделе проводимого лечения уровень гемоглобина снизился и составил 9,5 мг/дл, в связи с чем было произведено снижение доза рибавирина до 500 мг в сутки. На 10-й неделе пациент начал предъявлять жалобы на зуд в ладонях, подошвах ног, изгибах и складках поверхности живота, сопровождающихся чешуйчатыми повреждениями в данных области.
При этом, пациент отрицал чувство озноба, жара, респираторных симптомов или других проявлений. При физикальном обследовании мы отметили эритематозные, зудящие, чешуйчатые и шелушащиеся поражения рук, ног и живота (рис. 1А и 1В). Были назначены кортикостероиды местного действия и пероральный антигистаминный препарат что дало частичное улучшение описанных состояний.
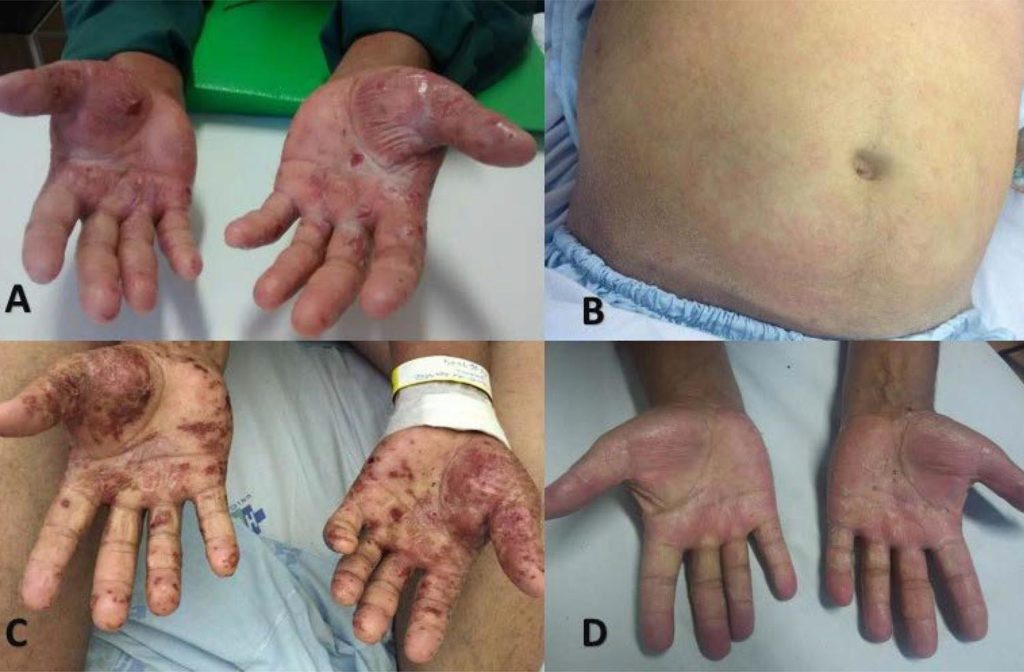
Спустя неделю после окончания лечения у него наблюдалась диффузная эритродермия с прогрессированием очагов поражения, вздутие волдырей на верхних и нижних конечностях, особенно на руках и ногах с участками шелушения, разрыв волдырей, трещины кожи с кровоточивостью и признаками вторичной инфекции ( рис.1С).
Мы начали амбулаторное лечение пероральным приемом преднизона в дозе 40 мг в день и цефалексином (цефалоспорин первого поколения) по 2 г в день. Несмотря на предпринимаемые меры поражения усиливались и данный пациент был госпитализирован в стационар. На момент госпитализации слизистые оболочки были чисты, не было никаких признаков лихорадки, эозинофилии или лимфаденопатии, а функции печени и почек сохранены. В связи с подозрением на фармакодермический характер поражения кожи с вторичной инфекцией было назначено лечение амоксициллином с клавулановой кислотой внутривенно и пероральный прием преднизолона по 60 мг ежедневно.
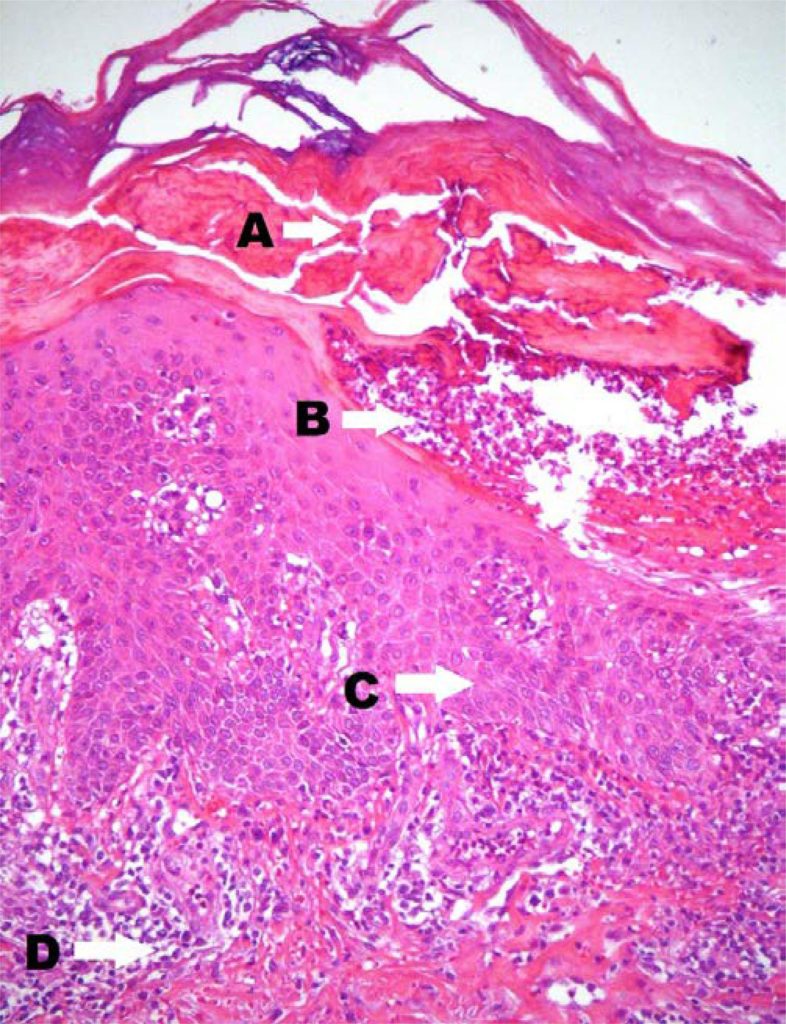
Биопсия кожи левой руки показала показала плоскоклеточный дерматит, подкорневую губчатую пустулу, псориазообразную гиперплазию эпидермиса и умеренный поверхностный смешанный воспалительный инфильтрат, состоящий из мононуклеарных лимфоцитов и эозинофилов (Рис.2). Полученные результаты явно указывали на фармакодермический характер поражения. Спустя неделю антибактериальной терапии с использованием высокой дозы преднизолона наблюдалось значительное улучшение состояния кожных покровов (рис.1D). Пациент был выписан, а доза преднизолона снижена до 10 мг.
Во время тщательного опроса пациент сообщил о факте аналогичных проявлений фармакодермии более года назад приписываемой топирамату, которые были успешно купированы приемом преднизона в дозировке по 60 мг в день. На 4-й и 12-й неделе после окончания лечения РНК ВГС не была выявлена, что позволило утверждать о достижении пациентом устойчивого вирусологического ответа и успехе проводимой терапии.
Обсуждение
Мы одни из первых, кто сообщил о дерматологических проявлениях побочных эффектов (АЕ) во время лечения с использованием софосбувира, симепревира и рибавирина. Подобного рода нежелательные явления обычно наблюдались при использовании интерферона и ингибиторов протеазы первой волны — телапревира и боцепревира. В ранее проведенных когортных исследованиях сообщалось, что общая частота тяжелых побочных эффектов составляет 12%, а дерматологические проявления встречаются у 57% пациентов получавших вышеописанную схему на основе интерферона.
По нашему мнению, перед началом лечения ВГС следует пристально изучить анамнез и учитывать многочисленные факторы риска — такие проявления, такие как:
- криоглобулинемия
- кожная порфирий
- красный плоский лишай
- псориаз
- крапивница
- мультиформная эритема и другие виды васкулита.
Во время собственно противовирусной терапии всегда следует учитывать возможность возникновения описанных нами негативных реакций, и, если есть какие-либо сомнения, необходимо выполнить биопсию кожи.
Метаанализ с 4187 пациентами, получавшими пегилированный интерферон и рибавирин усиленный ПППД (телапревир, боцепревир, симепревир или софосбувир) показал частоту возникновения дерматологических проявлений 44,5%, 25,4%, 23,1% и 20,5% соответственно. Безусловно, ПППД без сочетания с интерфероном хорошо переносятся и имеют существенно меньше нежелательных последствий, но не исключает их полностью. Кроме того, применение симепревира может приводить к повышению фоточувствительности кожи и росту уровня непрямого гипербилирубина.
В американском исследовании с 836 пациентами имеющим 1 генотип и получавшими софосбувир и симепревир, в сочетании с рибавирином или без него, анемия встречалась в 29,6%, а астения в 26,5%, причем оба проявления были характерны и выражены для группы с применением рибавирина. Серьезные нежелательные явления имели место у 5,3%, чаще встречались у пациентов с циррозом печени, которые составили почти 60% исследуемой популяции. При этом, существенных дерматологических проявлений выявлено не было.
Simpson сообщил о двух случаях тяжелых дерматологических проявлений вызванных применением софосбувира и симепревира спустя две и четыре недели после начала лечения. Первый из пациентов имел в анамнезе витилиго и аллергические реакции на ампициллин, а так же различные морепродукты. Второй пациент не имел отягощенного аллергоанамнеза. При этом ни у одного из них не было рибавирина в схеме лечения ВГС. Eyre также сообщал о фотоиндуцированном поражении кожи на второй неделе лечения софосбувиром и симепревиром у пациента после трансплантации печени, который получил существенное улучшением состояния после применения стероидов. Wang описал случай с проявлениями аналогичными описанными нами в данной статье, индуцированые софосбувиром и даклатасвиром у пациента анамнез которого был отягощен вульгарным псориазом и аллергией на Ко-тримоксазол.
В тех немногочисленных отчетах и описаниях, имеющихся на данный момент, все случаи имели корреляцию и совпадения по ряду признаков — все поврежденные участки кожи, располагались главным образом в местах, подверженных воздействию солнечного света, при этом, все пациенты имели в анамнезе аллергические реакции на продукты питания или лекарственные средства, а так же дерматологические заболевания или различные формы васкулита до начала лечения гепатита С.
Безусловно, существует ряд терапевтических мер воздействия для пациентов аналогичных групп с риском фармакодермии, не связанной с лечением ВГС. При этом, мы не знаем, могут ли быть экстраполированы эти меры на пациентов с ВГС и дерматологическими проявлениями вызванными применением ПППД.
К примеру, ряд исследователей сообщил что при ладонно-подошвенном синдроме связанным с применением доцетаксела для лечения рака молочной железы, весьма эффективно использование витамина Е и целекоксиба. В то же время, для пациентов с гепатоцеллюлярной карциномой которым проводиться лечение с использованием сорафениба, витамин Е способен улучшать состояние кожных покровов и уменьшать нежелательные дерматологические проявления без снижения дозы химиотерапии.
На наш взгляд, ввиду того что, на момент публикации статьи, отсутствуют сообщения о принятии какой-либо стратегии для предотвращения дерматологических проявлений вызванных ПППД, врачам следует акцентировать внимание не только на на самых первых проявлениях, но и проводить детальное исследование аллергоанамнеза до начала лечения гепатита С.
Источник: Hand-foot syndrome due to hepatitis C therapy.
Revista da Associação Médica Brasileira.
Rev. Assoc. Med. Bras. vol.64 no.5 São Paulo.
ISSN 1806-9282
Коллектив авторов: Daniel Mazo, Raquel Arrelaro, Nayana Vaz, Marcello Rabello, Tirzah Lopes, Bárbara Corrêa, Ana Beatriz Torino, Maria Cintra, Sonia Lorena, Tiago Sevá-Pereira, Jazon Almeida
- Department of Gastroenterology, School of Medical Sciences, University of Campinas (UNICAMP), Campinas, SP, Brasil
- Department of Gastroenterology, University of Sao Paulo School of Medicine (FMUSP), São Paulo, SP, Brasil
- Department of Dermatology, School of Medical Sciences, University of Campinas (UNICAMP), Campinas, SP, Brasil
Остались вопросы? Получите ответ на форуме
Имеются противопоказания! Необходима консультация специалиста.