Введение
COVID-19 относится к семейству бета-коронавирусов, которые несут ответственность за возникновение тяжелого острого (SARS HCoV) и ближневосточного (MERS HCoV) респираторных синдромов. До сегодняшнего дня сообщалось о шести различных штаммах коронавируса человека (HCoV) в дополнение к недавно выявленному COVID-19. Штаммы 229E и NL63 HCoV принадлежат к альфа-коронавирусам, а штаммы OC43, HKU1, SARS, MERS и COVID-19 относятся к бета-коронавирусам. SARS и MERS HCoV являются наиболее агрессивными штаммами. По данным ВОЗ, уровень смертности от SARS HCoV составляет 10%, а у MERS HCoV — 36%.
HCoV, как правило, представляют собой одноцепочечные РНК-вирусы с положительной цепью, очень длинной последовательностью (30000 п.н.) и характеризуются двумя группами белков: структурные, такие как Spike (S), Nucleocapsid (N) Matrix (M) и Envelope (E), и неструктурные белки, такие как РНК-зависимая РНК-полимераза (RdRp) (nsp12). RdRp является важнейшим ферментом в жизненном цикле РНК содержащих вирусов, включая семейство коронавирусов, вирус гепатита С (ВГС) и вирус Зика (ZIKV). Активный центр RdRp высококонсервативен и представляет собой два последовательных остатка аспартата, выступающих из структуры бета-витка, что делает поверхность доступной через нуклеотидный канал (свободные нуклеотиды могут проходить сквозь него).
В прошлом месяце в Китае было начато несколько in vitro и клинических испытаний первого одобренного Национальным управлением по лекарственным средствам Китая (18 февраля 2020 года) лекарственного препарата — Фавилавира. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов одобрило различные противовирусные препараты прямого действия против вируса гепатита С (ВГС), такие как Софосбувир и Рибавирин для применения с целью подавления RdRp. Эти препараты являются производными нуклеотидов, конкурирующих за активный центр RdRp. Полумаксимальная эффективная концентрация (ЕС50) для рибавирина по отношению к COVID-19 составляет 109,5 мкМ, тогда как его половинная максимальная концентрация ингибирования (IC50) вируса Денге составляет 8 мкМ. Софосбувир демонстрирует 4 мкМ против вируса Зика. Ремдесивир показывает EC90 1,76 мкМ против COVID-19 in vitro.
В настоящем исследовании из-за убедительных доказательств успешного ингибирования RdRp мы сфокусировали свое внимание на доступных в широкой практике нуклеотидных ингибиторах. Модель COVID-19 RdRp построена гомологическим образом после сравнения известных последовательностей с доступными структурами в банке данных протеома. Затем проводили многомерное моделирование молекулярного взаимодействия для оценки некоторых противовирусных препаратов прямого действия (ПППД) (Софосбувир, Рибавирин, Ремидисвир, IDX-184) в отношении COVID-19 RdRp. Результаты носят многообещающий характер и предполагают подавление РНК-полимеразы коронавируса доступными в настоящее время терапевтическими средствами.
Результаты и обсуждение
Моделирование RdRp COVID-19
Рисунок 1 А показывает множественное выравнивание последовательностей (MSA) РНК-зависимых РНК-полимераз из различных штаммов HCoV, включая альфа-коронавирусы (229E и NL63) и бета-коронавирусы (OC43, HKU1, SARS, MERS и COVID-19). Вторичная структура SARS HCoV показана в верхней части MSA (PDB ID: 6NUR, chain A), в то время как ее доступность находится в нижней части MSA. Высокодоступные остатки находятся в синих блоках, в то время как скрытые и недоступные остатки представлены белым цветом в нижней части. Прямоугольник с черными штрихами отмечает остатки активных центров (последовательные остатки аспартата D255 и D256). Активные аспартаты центра выступают из бета-поворота в β15 и β16. Как следует из MSA, активный центр имеет сильный уровень консервативности. Кроме того, область 5 Å, окружающая D255 и D256, имеет сильное сродство для всех HCoV, как показано синими пунктирными прямоугольниками. Эта область включает в себя Y114, C117, N186, N190, M251, I252, L253, S254, A257, V258, E306, F307, C308 и S309. Остатки активного центра и большая часть окружающей его области 5 Å являются поверхностно доступными, хотя и могут связываться со свободными нуклеотидами (ATP, GTP, CTP и UTP).
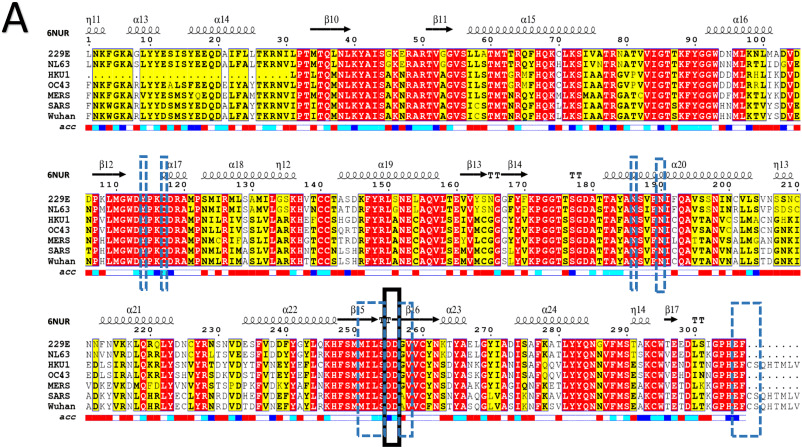
Для COVID-19 RdRp процентная идентичность последовательности по сравнению со штаммами SARS, MERS, OC43, NL63, 229E и HKU1 HCoV составляет 90.18%, 56.76%, 55.07%, 48.79%, 48.55%, и 48,16% соответственно. Таким образом, SARS HCoV RdRp является наиболее близким штаммом к COVID-19. Полный геном Wuhan SARS-like HCoV имеет идентичность последовательности 89,12% и 82,34% с изолятом Bat SARS-like coronavirus bat-SL-CoVZC45 и коронавирусом SARS ZS-C соответственно.
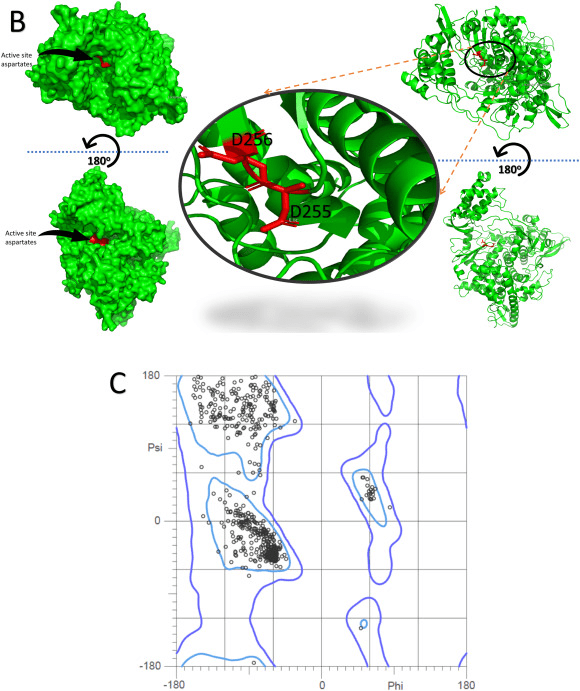
Модель COVID-19 RdRp (801 остаток) построена с помощью автоматизированного моделирования гомологии с использованием SARS HCoV RdRp (PDB ID: 6NUR, chain A) в качестве гомолога и имеет очень высокую (97,08%) идентичность последовательности, что говорит о её высоком качестве. Карта Рамачандрана показывает 100% остатков в разрешенных регионах, 97,5% — в наиболее благоприятном регионе (рис. 1С). Кроме того, 89,9% остатков имеют средний балл 3D-1D ≤ 0,2 полученный с использованием программного обеспечения Verify 3D, в то время как общий коэффициент качества ERRAT составляет 95,9%.
Взаимодействие ПППД и COVID-19 RdRp
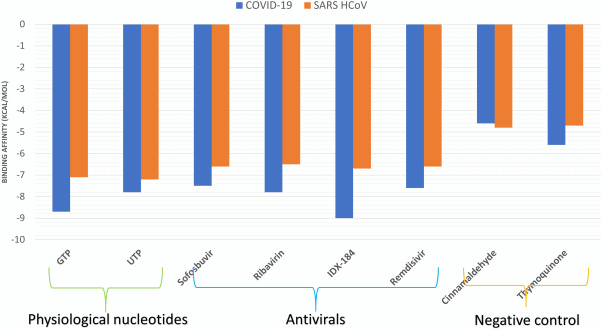
Перед проведением докинг-исследования получают структуры малых молекул, которые должны находиться в оптимизированной трифосфатной форме. Оптимизация выполняется с использованием силового поля MM3, затем PM6, после чего дальнейшая оптимизация выполняется с помощью теории функционала плотности B3LYP (DFT) основанной на методах расчёта электронной структуры систем квантовой физики и химии. Активный центр аспартата D255 и D256 во время эксперимента стыковки обрабатываются в качестве гибкой структуры. При стыковке с помощью инструментов AutoDock используется сеточный блок размером 30 × 30 × 30 Å с центром в точке (x, y, z) (142.1, 138.7, 150.0) Å. AutoDock Vina использует свою функцию подсчета очков (Vina) для прогнозирования взаимодействия между вышеупомянутыми лигандами и активным центром RdRp. На рис. 2 показаны значения баллов стыковки для COVID-19 (синие столбцы) и SARS HCoVs (оранжевые столбцы). Решенная структура SARS (PDB ID: 6NUR, chain A) используется для стыковки тех же лигандов, чтобы сравнить его энергию связи с энергией связи COVID-19 RdRp. Сеточный блок (30 × 30 × 30 Å) для SARS RdRp центрируется на (141.2, 138.5, 149.4) Å. Как видно из результатов докинга, восемь соединений, включая физиологические GTP и UTP, а также четыре препарата IDX-184, Софосбувир, Рибавирин и Ремидисвир, могут связываться как с COVID-19, так и с SARS HCoV RdRps с хорошей энергией связывания (от -6,5 до -9,0 ккал/моль). Несмотря на то, что SARS HCoV RdRp показывают несколько более высокие энергии связывания по сравнению с COVID-19 RdRp, разница все еще незначительна для Рибавирина, Ремдисивира, Софосбувира и его родительского нуклеотида UTP. В среднем 0,95 ккал / моль — это разница между энергиями связывания SARS и COVID-19 RdRp для данных соединений. С другой стороны, разница между энергиями связывания COVID-19 и SARS HCoV RdRps с IDX-184 и его родительским нуклеотидом GTP составляет 2,3 и 1,6 ккал/моль соответственно. Кроме того, все испытанные соединения показывают более низкие (лучшие) энергии связывания с COVID-19 RdRp по сравнению с SARS RdRp. Соединения используемые в качестве контроля (циннамальдегид и тимохинон) демонстрируют более низкое связывающее сродство к SARS и COVID-19 RdRp (выше -5,6 ккал/моль).
Чтобы проверить возможную причину различий в энергии связей, мы исследовали комплексы взаимодействия, образовавшиеся после стыковки с помощью PLIP. На рис. 3 показаны сформированные взаимодействия между препаратами ПППД и RdRp COVID-19 после стыковки, чтобы отразить связывающую силу под каждым комплексом указаны баллы. Лиганды окрашены в оранжевый цвет, в то время как белковые остатки представлены голубым. Водородные связи представляют собой сплошные синие линии, в то время как пунктирные линии представляют гидрофобные взаимодействия. В случае IDX-184 с D514 образуется только один солевой мостик (желтые сферы, соединенные пунктирной линией), который отвечает за повышенную стабилизацию образовавшегося комплекса. Количество водородных связей для IDX-184, софосбувира и рибавирина составляет 11, 7 и 13 соответственно. С другой стороны, IDX-184 и Софосбувир образуют связь между Mg+2 и D652 (два взаимодействия) и E702, соответственно. Это является еще одной причиной стабильности образовавшихся комплексов для IDX-184 и Софосбувира. Кроме того, Софосбувир образовал два гидрофобных взаимодействия с Y510 и D651 RDRP COVID-19.
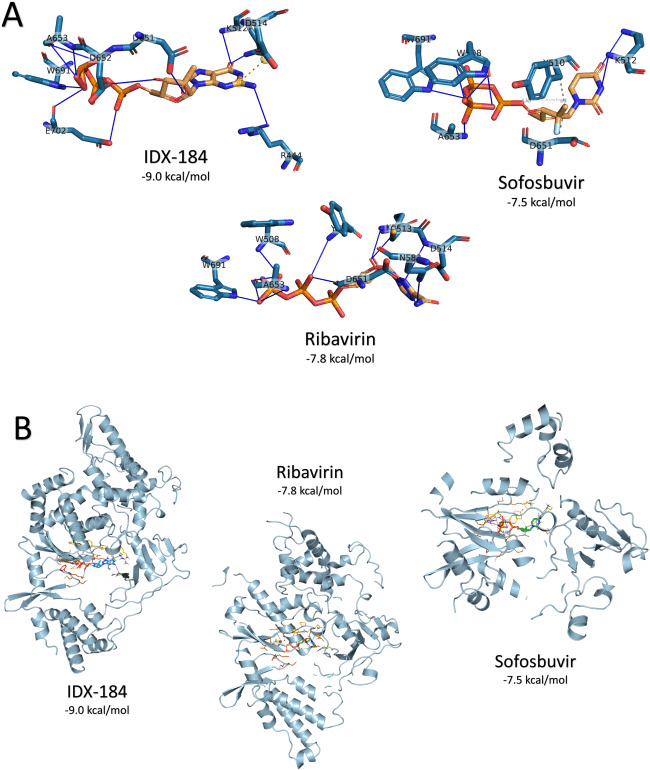
Подводя итог вышеизложенному, можно сказать, что IDX-184, Софосбувир и Рибавирин могут образовывать плотную связь с RdRp, и, следовательно, нарушать функции важного белка, что приводит к эрадикации вирусной популяции. Кроме того, IDX-184 показывает лучшие результаты в сравнении с Софосбувиром в качестве мощного ингибитора RdRp недавно появившегося штамма COVID-19 HCoV. Дальнейшая изучение взаимодействия вышеупомянутых соединений может привести к получению более мощного препарата, способного остановить вновь возникшее инфекционное заболевание.
Вывод
Возникновение нового штамма коронавируса в городе Ухань вызывает повышенную озабоченность здравоохранения с момента последней вспышки SARS в 2002-2003 году, оставившей более 700 смертей и 8000 случаев заболевания только в Китае. Кроме того, аналогичная вспышка в ближневосточном регионе в результате которой более 800 человек погибли и 2500 были госпитализированы имела совершенно иную картину инфицирования (MERS). Настоящее исследование было направлено на то, чтобы проверить возможность применения препаратов ПППД, которые широко применяются в медицинской практике. Софосбувир, Рибавирин и Ремдисивир демонстрируют многообещающие результаты и могут быть использованы против нового штамма COVID-19.
Источники:
- Anti-HCV, nucleotide inhibitors, repurposing against COVID-19
- Life Sciences. Volume 248, 1 May 2020, 117477
- https://doi.org/10.1016/j.lfs.2020.117477
Автор: Abdo A. Elfiky. Biophysics Department, Faculty of Sciences, Cairo University, Giza, Egypt. College of Applied Medical Sciences, University of Al-Jouf, Saudi Arabia