Введение
Хронический вирусный гепатит C (HCV) связан с прогрессирующим заболеванием печени, которое может привести к циррозу и гепатоцеллюлярной карциноме. По оценкам текущих эпидемиологических исследований, 130-150 миллионов человек во всем мире инфицированы HCV, в результате чего ежегодно умирает до 350 000 человек. В Тайване около 578 000 человек инфицированы HCV, а наиболее распространенным генотипом является генотип 1b, на который приходится более 50% всех инфекций.
В последние несколько десятилетий комбинированная терапия peg-inf и RBV достигает показателей SVR12 порядка 40-50% у пациентов с 1b генотипом, при этом связана со значительными побочными эффектами. В 2011 году в клиническую практику были введены первые противовирусные препараты прямого действия (DAAs) — boceprevir и telaprevir. В западных странах, эти препараты первоначально были одобрены для 1 генотипа в комбинации с peg-inf и RBV. Тем не менее, ввиду тяжелых лекарственных взаимодействий использование ингибиторов протеазы первого поколения было значительно ограничено. Позже появились схемы sofosbuvir/RBV и sofosbuvir/ledipasvir которые были одобрены в качестве пероральных анти-HCV агентов для 1, 2 и 4 генотипов. В конце июня 2016, FDA одобрило применение epclusa (sofosbuvir 400mg/velpatasvir 100mg) в качестве рекомендованного комбинированного пангенотипического препарата.
Между тем, в Северо-Восточной Азии, первые одобренные DAAs это — daclatasvir (DCV) и asunaprevir (ASV) в Японии и Корее. DCV является ингибитором NS5А с активностью в отношении HCV генотипов 1-6 in vitro, а ASV-это ингибитор протеазы NS3 с активностью в отношении 1, 4, 5, 6 генотипов. Все безинтерфероновые комбинации DCV и ASV хорошо переносятся и обеспечили достижение SVR порядка ∼90% для пациентов с 1b-генотипом. В тоже время среди пациентов с данным генотипом, частота ингибитор-резистентных вариантов NS5A составляет около 4-5% во всем мире, но в Японии, к сожалению, этот показатель доходит до 11-23%.
Поскольку вероятность достижения SVR у группы пациентов с отсутствием ответа или рецидивом связана прежде всего с полиморфизмом NS5A-Y93H, то обнаружение RAV перед терапией было бы полезно в качестве фактора облегчающего прогнозирование ответа на терапию. Распределение генотипов HCV на Тайване аналогично Японии, причем основным является 1b генотип. Для пациентов с базовой устойчивостью NS5A в настоящее время существует много новых препаратов (sofosbuvir+ledipasvir или Viekira PAK включающий в себя ombitasvir, paritaprevir, ритонавир/дасабувир). Однако применение этих препаратов по-прежнему затруднительно ввиду дороговизны. Поэтому мы решили оценить возможность добавления RBV для улучшения прогноза исхода терапии. Недавнее исследование, в котором приняли участие девять из десяти пациентов с коинфекцией HIV/ HCV, которые не достигли SVR после терапии LED+SOF, свидетельствовало о существенной роли RBV. После рецидива у семи пациентов была выявлена устойчивость NS5A. Несмотря на это, девять рецидивирующих пациентов прошли повторный курс sof+led длительностью 24 недели с добавлением RBV. Восемь из девяти (89%) пациентов достигли SVR12. Результаты предполагают, что добавление RBV может повышать эффективность терапии у пациентов с устойчивостью NS5A в комбинации как DCV, так и с ASV.
Пациенты и методы
Это открытое исследование было проведено в Национальной Больнице Тайваньского Университета. Критериями исключения для были пациенты с клиническими или биохимическими доказательствами декомпенсированного цирроза, наличия гепатоцеллюлярной карциномы. DCV вводили перорально в дозе 60 мг один раз в день, в тоже время ASV вводили перорально в дозе 100 мг два раза в день. Из шести пациентов четверо были мужчинами, а двое — женщинами. У четырех пациентов был негативный опыт лечения пегилированным интерфероном и RBV, а два до этого терапию не проходили. Кроме того у двух пациентов в группе был компенсированный цирроз печени. Среди этих шести пациентов был обнаружен полиморфизм NS5A-Y93H, но не был обнаружен NS5A L31. RBV использовали в течение 24 недель во время терапии и через 12 недель после лечения.
Первичной точкой оценки эффективности была необнаруживаемая РНК через 12 недель после окончания лечения (SVR12) при уровне чувствительности анализатора в пределах <25 МЕ/мл.
Все пациенты были допущены к терапии после тщательного физического осмотра, путем анализа возможных неблагоприятных событий исходя из их анамнеза, а так же клинических лабораторных исследований крови после 1-ого дня лечения, на 12-й, 16-й и 20-й неделях, а так же в конце терапии.
Определение полиморфизма HC5 NS5A N31 и Y95. Вариант аминокислотной замены связанный с лекарственной устойчивостью в NS5A выясняли с помощью прямого секвенирования.
Результаты
Все пациенты были жителями Тайваня. Средний возраст пациентов (6 случаев: 4 мужчины и 2 женщины) составил 68 лет (таблица 1). У всех пациентов была замена Y93H, при этом замена L31 обнаружена не была.
| Sex | Age (y) | Treatment naïve/ experienced | Liver cirrhosis | NS5A RAV | RBV | Baseline HCV RNA (IU/ mL) | ALT (U/L) | Cre (mg/dL) | Treatment start date | VR24 | SVR12 | |
| 1a | M | 62 | TE | Y | Y93H/L31 | Y | 1,980,000 | 30 | 10.12.2015 | 2,560,000 | ||
| 2b | F | 68 | TE | Y | Y93H(mixed)/L31 | Y | 321 | 121 | 17.12.2015 | UD | ||
| 3 | M | 72 | TN | N | Y93H/L31 | Y | 1,250,000 | 23 | 27.10.2015 | UD | ||
| 4 | M | 76 | TE | N | Y93H/L31 | Y | 4,960,000 | 18 | 10.03.2015 | UD | ||
| 5 | F | 63 | TN | N | Y93H/L31 | Y | 1,470,000 | 80 | 0.5 | 10.03.2015 | UD | |
| 6 | M | 48 | TE | N | Y93H/L31 | Y | 1,279,989 | 48 | 02.12.2014 | UD |
ALT = аланиновая трансаминаза; Cre = креатинин; F = женщина; HCV = вирус гепатита С; M = мужчина; RAV = варианты, связанные с устойчивостью; SVR = УВО, устойчивый вирусологический ответ; TE = есть предыдущий опыт лечения; TN = ранее терапию не проходил; UD = РНК не обнаруживается; Y = да. a — рецидив b — пациент ранее проходил терапию по поводу гепатоцеллюлярной карциномы.
Побочные эффекты, ведущие к прекращению терапии
В целом, ни один из пациентов не прекратил лечение из-за неблагоприятных побочных эффектов. Среди пациентов с добавлением RBV отмечались некоторые незначительные побочные эффекты, такие как кожный зуд, умеренная лихорадка, снижение гематокрита и сухость кожных покровов. Не было отмечено ни одного случая серьезных побочных эффектов которые могли бы привести к смерти пациента.
Клинические результаты
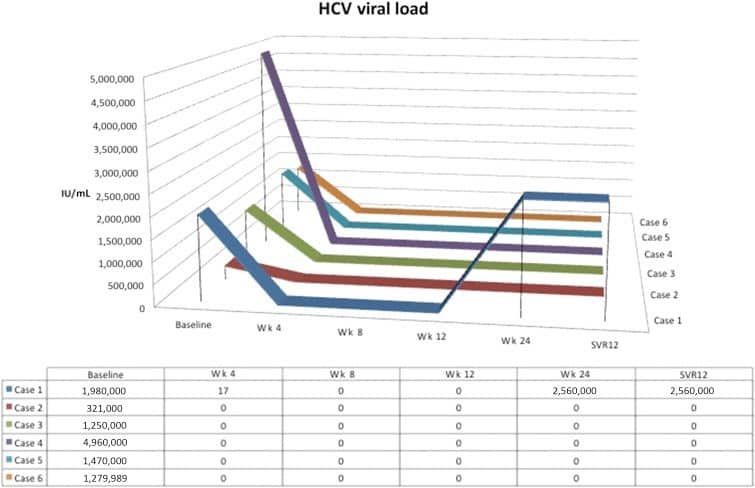
В пяти случаях РНК HCV были неопределяемыми на 12-й неделе после терапии (рис. 1). Однако вирусная нагрузка одного пациента достигла нуля на 12-й неделе, но затем восстановилась и возросла до 2.560.000 МЕ/мл на 24-й неделе лечения. Пациент с вирусологическим прорывом имел цирроз печени и опыт неудачного лечения.
Обсуждение
С появлением противовирусных агентов прямого действия лечение хронического гепатита С вышло на принципиально новый уровень, и в целом наблюдается удовлетворительное достижение SVR. Однако еще предстоит преодолеть большое количество препятствий. Появление RAV является одной из основных проблем. На сегодняшний день руководства по лечению пациентов с лекарственной устойчивостью не разработаны. Так, скажем в последнем японском руководстве рекомендуется провести предварительный анализ RAVs NS5A L31 / Y93 перед терапией DSV+ASV, в то время как Европейская Ассоциация по Изучению Печени и Американской Ассоциации по Изучению Болезней Печени рекомендаций по лечению заболеваний печени не рекомендует тестирование на устойчивость, за исключением NS3 Q80K в случае проведения терапии на основе симепревира ввиду того что схема DSV+ASV не была одобрена в Европе и США. Тем не менее, в Американской ассоциации рекомендуется провести тестирование резистентности к лекарственным средствам перед повторным лечением пациентов, у которых предшествующая терапия не удалась, хотя конкретные рекомендации не предоставляются. Лучшую стратегию терапии еще предстоит разработать, а для этого потребуется больше клинических исследований. В регионах и странах с ограниченными ресурсами неудовлетворенная потребность еще более значительно выражена по финансовой причине — новые DAAs для развивающихся регионов являются очень дорогостоящими.
Наше исследование о клиническом опыте добавления RBV к двойной терапии ASV+DSV для пациентов с 1b генотипом инфекции и устойчивостью NS5A в целом подтверждает оправданность этого. Хотя точный механизм и роль RBV пока неясна, было предложено несколько механизмов: прямое ингибирование вирусной РНК-полимеразы; или противовирусная активность, связанная с истощением внутриклеточных гуанозинтрифосфатных пулов , вызванная ингибированием фермента инозинмонофосфатдегидрогеназы. Кроме того, были изучены мутагенные свойства RBV, приводящие к «катастрофе накопления ошибок». Недавнее исследование показало, что RBV оказывает мутагенное действие на HCV путем индуцирования нуклеотидных переходов, что указывает на то, что этот эффект может быть важным фактором, объясняющим противовирусную активность RBV. Таким образом, RBV может действовать через различные механизмы: (1) прямая противовирусная активность частично объясняется мутагенными свойствами; и (2) косвенный биохимический эффект через неизвестный нам механизм. Предварительные результаты предполагают, что дальнейшее исследование имеет важное значение, особенно в районах с ограниченными ресурсами.
Что касается побочных эффектов, были отмечены некоторые незначительные побочные эффекты, таких как: кожный зуд, умеренная лихорадка, анемия, сухость кожи и покраснение лица. Побочные эффекты могут быть связаны с RBV. Пациенты нормально переносили побочные эффекты и речь о рекращении терапии не шла. Никаких серьезных побочных эффектов или смерти в результате них зафиксировано не было.
Наше исследование имеет ценность для ограниченных ресурсами регионов и развивающихся стран. Добавление RBV может быть экономически-оправданной стратегией для пациентов с устойчивой формой NS5A.
Таким образом, предварительные результаты проведенного исследования показывают, что добавление RBV может улучшить показатели RSV у пациентов с 1b генотипом и устойчивостью NS5A. Однако из-за малого объема пациентов в нашем исследовании результаты должны быть подтверждены другими клиническими испытаниями.
Источник:
Journal of the Formosan Medical Association. Volume 116, Issue 4, April 2017 , Pages 295-299 http://www.jfma-online.com/article/S0929-6646(16)30436-3/fulltext
Коллектив авторов:
Chun-MingHonga, Chun-JenLiub, Shiou-HweiYehc, Pei-JerChena
a — Department of Traumatology, National Taiwan University Hospital, Taipei, Taiwan
b — Department of Internal Medicine and Hepatitis Research Center, National Taiwan University Hospital, Taipei, Taiwan
c — Department of Microbiology, College of Medicine, National Taiwan University, Taipei, Taiwan
Похожие статьи:
- Химерный вирус генотипа 2k/1b и его лечение
Статья целиком: Происхождение, распространенность и ответ на терапию гепатита C, вызванного химерным вирусом генотипа 2k/1b Актуальность…
- Лечение гепатита С: Софосбувир и Даклатасвир
Прежде чем выяснить как правильно пить Софосбувир Даклатасвир, следует ознакомиться с общей информацией об этих…
- Даклатасвир инструкция по применению
Содержание: Показания к применению Способ применения Схема лечения Противопоказания Побочное действие Взаимодействие с другими лекарственными…
Имеются противопоказания! Необходима консультация специалиста